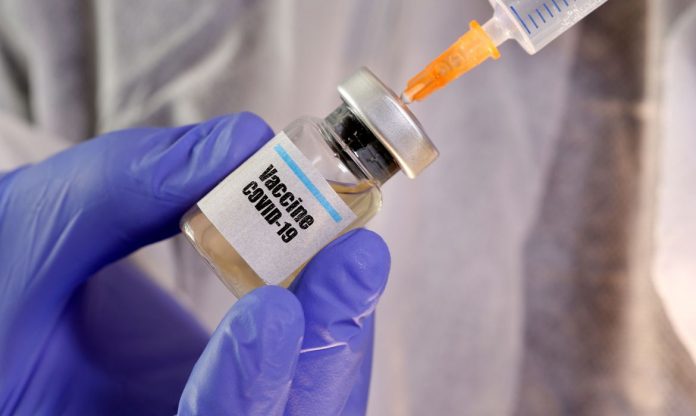
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na tarde deste domingo, os dois pedidos para liberação do uso emergencial das vacinas CoronaVac e Oxford contra o coronavírus. Os imunizantes são desenvolvidos pelo Instituto Butantan e pela Fundação Oswaldo Cruz (Fiocruz). Com reunião que durou aproximadamente 5 horas, os votos foram unânimes pelos cinco diretores da agência.
Os diretores seguiram o voto de Meiruze Freitas, relatora dos pedidos para uso emergencial das vacinas, que foi a primeira a votar. Em seguida, foi a vez de Romison Mota, depois de Alex Campos, Cristiane Gomes e, por fim, presidente da Anvisa, Antônio Barra Torres. As decisões serão publicadas e comunicadas às duas instituições ainda neste domingo. No caso da CoronaVac, a autorização foi condicionada ainda à assinatura de um Termo de Compromisso e sua respectiva publicação no Diário Oficial da União (DOU).
O termo de compromisso prevê que, até o dia 28 de fevereiro, seja enviado para Anvisa a complementação dos estudos de imunogenicidade, como uma das condições da relatora dos pedidos. A chamada imunogenicidade é a capacidade, por exemplo, de uma vacina incentivar o organismo a produzir anticorpos contra o agente causador da doença.
Esse documento, portanto, deve complementar as informações referentes à imunidade conferida aos voluntários que receberam a vacina na terceira fase de desenvolvimento clínico. O dado é imprescindível para que se possa concluir a duração da resposta imunológica nos indivíduos vacinados.
Ao votar, Meiruze afirmou a necessidade de ter uma vacina aprovada para combater a pandemia do coronavírus no país. “É certo que a avaliação de eficácia de uma vacina é complexa para muitas doenças. Mas é certo que para covid-19, em que a compreensão do vírus ainda está evoluindo, a complexidade aumenta ainda mais. Sabemos que para o Brasil, com suas especificações epidemiológicas, os desafios próprios do enfrentamento da pandemia é essencial que haja vacinas o quanto antes”, afirmou Meiruze.
Além disso, a diretora ressaltou a importância das medidas de distanciamento social até que boa parte da população seja imunizada. “Reconheço um marco histórico e a contribuição valorosa da autorização do uso emergencial da vacina no enfrentamento da pandemia. Ressalto ainda o caráter decisivo das medidas de proteção e distanciamento social neste momento, em especial até que uma quantidade de vacinas estejam suficientes e significativas para a população brasileira”, disse ela.
Ao contrário das autoridades brasileiras que defendem o tratamento precoce com medicamentos que não foram comprovados cientificamente, diretores pontuaram que não existe qualquer indicação para cura da covid-19. “Até o momento, não contamos com alternativa terapêutica comprovada disponível para prevenir ou tratar o novo coronavírus”, disse Meiruze.
Ao confirmar o resultado da liberação emergencial das vacinas, o diretor-presidente da Anvisa afirmou que a imunização da vacina demora algum tempo para ocorrer. Por isso, mesmo ao receber as doses, os brasileiros precisam usar máscara, manter o distanciamento social e higienizar as mãos.
Reportagem: Redação Amazônia sem Fronteiras